iPS细胞“复刻”胸腺!京都大学突破:体外重现人类胸腺发育,免疫缺陷治疗迎来新曙光
来源:生物谷原创 2025-08-28 09:00
研究团队设计了一套化学成分明确的诱导方案,让iPS 细胞一步步“变身”为成熟T 细胞(TEC)。

在一项新的研究中,由京都大学 Yoko Hamazaki 教授和 Yann Pretemer 助理教授领导的研究团队,用诱导性多能干细胞(iPS 细胞)实现了一项关键突破——他们开发出完全体外的培养系统,能忠实重现人类胸腺上皮细胞(TEC)从早期发育到终末成熟的全过程。
这项发表在《Nature Communications》的成果,不仅填补了人类胸腺器官发生研究的空白,更为免疫缺陷疾病(如迪乔治综合征)的治疗、功能性 T 细胞的体外制备打开了新大门。

胸腺是免疫系统的 “训练基地”:它通过TEC构建的微环境,指导未成熟胸腺细胞(胸腺细胞)分化为能区分 “自我” 与 “非我” 的成熟T 细胞—— 皮质TEC(cTEC)负责筛选能识别外来抗原的T 细胞(阳性选择),髓质TEC(mTEC)则清除会攻击自身组织的T 细胞(阴性选择),而AIRE蛋白是mTEC实现自我耐受的核心分子。但TEC高度异质性且极难从人体分离 —— 尤其是胚胎发育阶段的TEC,加上小鼠模型与人类胸腺在 gestation 时间、形态(如人类特有的哈氏小体)上差异显著,原代TEC体外培养又会快速丢失关键基因(如FOXN1),这些都让人类胸腺发育机制研究长期受限。
为突破这些瓶颈,研究团队设计了一套化学成分明确的诱导方案,让iPS 细胞一步步 “变身” 为TEC:首先用Activin A、CHIR99021等因子引导iPS 细胞分化为定形内胚层(DE),再通过BMP抑制剂LDN-193189和TGFβ抑制剂A-83-01诱导出前肠前段内胚层(AFE)——这是胸腺、甲状腺等咽器官的共同前体。
最关键的一步在第 7 天:团队加入视黄酸(RA)和FGF8,RA精准调控HOXA3基因(指定胸腺起源的第三咽囊位置)的表达,FGF8则促进咽结构发育,最终在第 28 天诱导出FOXN1⁺ TEC祖细胞样细胞,其FOXN1表达量达到儿科捐赠者原代TEC的一半左右。
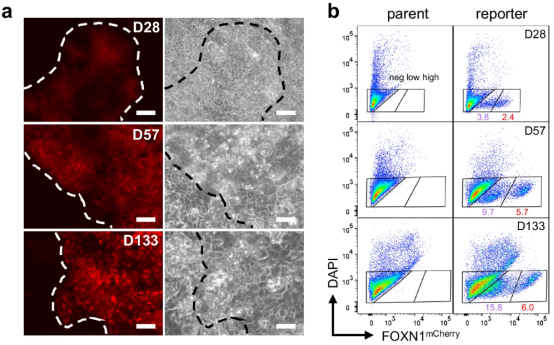
为实时追踪TEC发育,团队还构建了FOXN1-mCherry荧光报告iPS 细胞系——在FOXN1基因末端插入T2A-mCherry序列,只要FOXN1表达,细胞就会发出红色荧光。观察发现,第 28 天细胞首次出现微弱荧光;到第 57 天,荧光细胞分化为mCherryhigh和mCherrylow两个群体;直至第 133 天,mCherryhigh群体成为cTEC(高表达PSMB11、PRSS16等cTEC特异性蛋白,负责T 细胞阳性选择),mCherrylow群体则分化为mTEC(表达CCL19、CCL21等趋化因子,引导T 细胞向髓质迁移),甚至形成高度约 100μm 的 3D 结节,重现胸腺皮质与髓质的空间分隔结构。
更重要的是,这些诱导出的TEC(iTEC)具备完整功能。它们不仅表达IL-7(支持T 细胞存活)、DLL4(T 细胞分化关键配体)和MHC II类分子(CD4⁺ T 细胞选择必需),还能在与人类胸腺细胞共培养时 “训练” 出功能性T 细胞。团队将第 37 天的mCherry⁺ iTEC,与儿科捐赠者的双阳性(DP,即未成熟CD4⁺CD8⁺)胸腺细胞在气液界面类器官中共培养 2 周,结果令人惊喜:iTEC能将 91% 的DP细胞诱导为CD4⁺和CD8⁺单阳性(SP)成熟T 细胞,其中CD4⁺ SP占 47%、CD8⁺ SP占 21%,远优于传统的MS5-hDLL1细胞系(仅产生少量SP细胞)。这些SP细胞中,CD62L⁺CD45RA⁺CCR7⁺的 “初始T 细胞” 比例显著高于对照组,且TCRβ受体库的多样性与儿科供体的原代SP细胞高度相似(Shannon 指数接近),证明iTEC能完美复刻胸腺的 “训练” 功能。
共培养还推动了iTEC的终末成熟:原本未表达的AIRE基因,在共培养后上调至原代TEC的 6%,同时出现神经元样模拟性TEC(表达ASCL1、NEUROG1等神经分化标志物)和分泌细胞样模拟性TEC(表达SLPI、CXCL17等分泌蛋白)——这些模拟性TEC是胸腺实现 “自我耐受” 的关键,它们模仿胸腺外组织的抗原,提前让T 细胞“认识” 自身组织,避免 autoimmune 疾病。
单细胞 RNA 测序进一步验证了iTEC的 “真实性”:将第 133 天的iTEC与 3 名儿科捐赠者的原代胸腺基质细胞整合分析发现,iTEC的cTEC群体与原代cTEC完全 “共簇”,且共享LY75、DLL4等关键标志物;iTEC的mTEC则对应原代mTEC的不同亚型——mTEC I匹配分泌趋化因子的mTEC-CCL19/21,mTEC II匹配高表达MHC II的mTEC-CLDN3/4(含AIRE⁺细胞),mTEC III则是分泌细胞样模拟性TEC。基因调控网络分析还发现,ELF3、GRHL1、GRHL3等转录因子在mTEC分化中起核心作用,这与小鼠研究中这些因子调控FOXN1和模拟性TEC发育的结论一致,证明人类与小鼠的TEC发育机制存在共通性。
值得注意的是,培养体系中还自发出现了间充质样细胞(表达VIM),它们分泌BMP、FGF家族因子和胶原蛋白、层粘连蛋白等细胞外基质成分,通过“上皮 - 间质相互作用”为iTEC提供微环境支持——这正是iTEC能在 2D 培养中稳定维持FOXN1表达和功能长达 133 天的关键,而传统原代TEC在体外几天内就会丢失FOXN1。
这项研究的价值远超基础科学:对于迪乔治综合征、Pignata Guarino 综合征等先天性无胸腺症患者,目前唯一的治疗是胸腺移植,但面临供体稀缺、免疫排斥和移植后感染风险。而该系统可利用患者自身iPS 细胞诱导iTEC,再体外生成匹配MHC的功能性T 细胞,实现 “无排斥” 的免疫重建;对于化疗导致的胸腺损伤或衰老相关的胸腺萎缩,也可通过该模型筛选促进iTEC增殖的药物(如调控NF-κB、NOTCH信号的分子),推动胸腺再生。此外,它还能模拟先天性胸腺疾病的病理过程——比如FOXN1突变导致的 “裸鼠样” 表型,帮助科学家找到致病机制。
“这不仅是胸腺研究的突破,更是再生免疫医学的一步关键棋。” 研究团队表示,未来将进一步优化iTEC的成熟效率,推动其向临床转化,为更多免疫缺陷患者带来希望。(生物谷Bioon.com)
参考文献:
Yann Pretemer et al, An iPSC-based in vitro model recapitulates human thymic epithelial development and multi-lineage specification, Nature Communications (2025). DOI: 10.1038/s41467-025-62523-1.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


